第 15 章醛和酮
推荐文章:【有机化学】【有机化学目录】(https://jb243.github.io/pages/1483)
1. 概述
2. 亲核加成反应
3. 其他反应
4. 醛的合成方法
5. 酮合成方法
1.概述
⑴ 命名法
①醛命名法
○ 含有 CHO 的最长链是母体
○ CHO 中的醛碳编号为 1
○ 醛基为母体:以后缀-环烷甲醛命名
○ 链状结构中的醛被视为取代基:以oxo命名
○ 环结构中的醛被视为取代基:以甲酰基命名
○ 系统命名法(左)与通用命名法(右)的比较
○ 甲醛/甲醛
○ 乙醛/乙醛
○ 2-溴丙醛 / α-溴丙醛
○ 3-氯丁醛 / β-氯丁醛
○ 3-甲基丁醛/异戊醛
○ 十六醛 /
② 酮命名法
○ 含有 C=O 的最长链是母体
○ 最靠近 C=O 的链末端编号为 1
○ 附在环上的酮是母体:以后缀-环烷酮命名
○ 链状或环状结构中的酮被视为取代基:以oxo命名
○ 系统命名法(左)与通用命名法(右)的比较
○ 丙酮/丙酮、二甲基酮
○ 3-己酮/乙基丙基酮
○ 6-甲基-2-庚酮/甲基异己酮
○ 2,4-戊二酮/乙酰丙酮
○ 环己酮 /
○ 丁二酮 /
⑵ 常用反应原理
①亲核攻击、亲电攻击
② 质子转移:发生在分子间,而不是分子内
③ 互变平衡:烯醇 ↔ 酮
④ 后处理:用于纯化的有用关键字,无需指定确切的酸或碱
⑶ 反应性比较
①羰基化合物反应性比较
○ 酰卤 > 酸酐 > 醛 > 酮 > 酯~羧酸 > 酰胺 > 羧酸根离子
② 基于官能团的酮反应活性比较
图 1. 基于官能团的酮反应性比较
○ 醛比酮更具反应性、亲电性并且燃烧热更高
○ 原因1: 位阻:更多的取代基阻碍亲核攻击,降低亲核性
○ 原因2: 诱导效应:取代基通过超共轭为酮碳提供电子密度
③ 其他比较
○ 醛和酮的反应非常相似
○ 酮的极性比醛的极性大
○ 原因:酮通过甲基稳定共振贡献者中的碳正离子
○ 脂肪族酮比芳香族酮更具反应性
○ 氧化还原反应中醛类和酮类的反应活性存在差异
○ 原因:醛可以进一步氧化,而酮不能进一步氧化
○ 示例:银镜反应、费林反应、本尼迪克特反应仅与醛发生
2.亲核加成反应
⑴ 概述
① Bürgi-Dunitz 角:亲核试剂的 HOMO 接近羰基反键轨道 (LUMO) 的角度
②酸性条件:增加羰基的亲电性
③ 基本条件:增加亲核试剂的亲核性> ④ 卤离子对羰基化合物不充当亲核试剂
⑵ 类型1. 当Y-的碱度大于X-时
① 概述
○ 1 型 常见于酰氯中
○ 羧酸也经常表现出与类型 1 类似的行为
○ 醛和酮发生类型1反应的情况很少见
图 2. 羰基化合物反应类型 1
② 实施例1. 酰氯:Cl-的碱度很低
图3. 酰氯的反应
⑶ 类型2. 当Y-的碱度小于X-时
① 概述
○ 醛类和酮类大多遵循类型2
○ 其他反应通常涉及类型 2 的应用
图 4. 羰基化合物反应 类型 2
② 实施例1. 酸催化羰基加成反应
图 5. 酸催化的羰基加成反应
③ 实施例2. 碱催化的羰基加成反应
图 6. 碱催化的羰基加成反应
④ 实施例3. 缩醛形成反应:羰基碳保护反应
○ 缩醛和半缩醛
<img src =“https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2FlROzx%2Fbtrr6A1Sk1T%2FBAXoj7o2MwxC2Dp70m78fK%2Fimg.png” alt=”绘图”>
图 7. 半缩醛、乙缩醛、半缩酮和缩酮的结构
○ 反应机理:(式) 除去酮氧并附加两个-OR基团
图 8. 缩醛形成反应示例
○ 缩醛形成反应在相同条件下有逆反应
○ 迪安-斯达克阱去除 H2O,提高产率,因为 H2O 是反应产物
○ 溶剂:使用高沸点和恒沸点的甲苯、二甲苯等共沸溶剂( ∵ Dean-stark trap必要条件)
○ 过量的醇作为反应物会增加产率 → 通常添加过量而不是 2 当量
○ 酯、羧酸和酰胺在典型的酸性条件下不会形成缩醛
○ 示例 3-1.
图 9. 缩醛形成反应
○ 示例 3-2.
图10. 缩醛形成反应
○ 实施例3-3. Corey-Seebach反应:硫醇加成反应
图11. 硫醇加成反应
○ 还原反应:硫缩醛 + H2 / Raney-Ni(脱硫)
④ 实施例4. 胺加成反应
○ 机理: (式) 除去羰基(=O)并附着亚胺(=NR)
○ 由于逆反应也是可能的,因此在某一点达到平衡。
○ 亚胺在 pH 4-5 时形成最佳
○ 实施例4-1. 一般胺加成反应
图12. 醛和酮胺加成反应
○ 实施例4-2. 对甲苯磺酰肼(CH3-Ph-SO2NHNH2)
○ 实施例4-3. 烯胺形成反应
<img src =“https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2FuP4UJ%2Fbtrr9giS5vR%2FKb5aUvcUVrptK98Mm2me5K%2Fimg.png” alt=”绘图”>
图13. 烯胺形成反应
○ 与伯胺不同,仲胺缺少从亚胺离子上除去的质子,因此附着在 α 碳上的氢被除去。
○ 由于C=N键强度大于C=C键强度,因此在伯胺添加过程中会形成亚胺
○ 鹳-烯胺反应:烯胺作为亲核试剂与卤代烷、酰基卤、羰基化合物等发生反应。
○ 实施例4-4. NaBH3CN的还原反应:亚胺被还原为胺
图14. NaBH3CN的还原反应
○ 实施例4-5. 环状RNA合成:胺加成+NaBH3CN还原
图15. 环状RNA合成
○ 实施例4-6. Wolff-Kishner还原反应
○ NH2NH2,强碱(例如 KOH、NaOH),加热条件会导致额外还原
○ 用碱处理-C=N-NH2(腙)时
○ 示例4-7. 贝克曼重排
○ 用酸处理-C=N-OH(肟)时
○ 实施例 4-8. Pomeranz-Fritsch 反应
<img src =“https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2FcJQcCa%2FbtrXBkOyiu2%2FxbkFr2VH5XsbYxJLFXk7YK%2Fimg.png” alt=”绘图”>
图 16. Pomeranz-Fritsch 反应
○ 苯甲醛 + 2,2-二烷氧基乙胺进行胺加成反应和亲电芳香取代(EAS)
○ 实施例 4-9. Pictet-Spengler 反应
<img src =“https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2Ft1gWD%2FbtrXECfUVDl%2F82rmfNDQ9BYVUllN8meX8k%2Fimg.png” alt=”绘图”>
图 17. Pictet-Spengler 反应
○ 胺加成反应和Friedel-Crafts烷基化
⑤ 实施例5. 醛酮的HCN加成反应

○ 实施例5-1. 安息香缩合反应
○ 实施例5-2. Stetter反应
⑷ 类型3. 烯酮与1,2-加成反应
① 适用于亲核试剂为强亲核试剂(例如:格氏试剂)
② 机制
图19. 烯酮和1,2-加成反应的机理
⑸ 类型4. 烯酮和1,4-加成反应(迈克尔加成)
① 适用于亲核试剂为弱亲核试剂(例如:MeSH)
② 机制
图20. 烯酮和1,4-加成反应的机理
③ 例外:对于酰氯,即使使用弱亲核试剂也会发生 1,2-加成反应
图 21. 烯酮和酰氯
3。其他反应
⑴ 加氢反应
① 实施例1. 用金属试剂氢化
图 22. 通过添加金属试剂对醛和酮进行氢化
② 实施例2. Pd/C加氢反应:烯烃比酮更具反应性
图 23. H2(1 eq.)条件下的 Pd/C 氢化
图 24. H2(过量)条件下的 Pd/C 加氢
⑵ 氧化还原反应
① 实施例1. 有机金属试剂与醛、酮的反应
○ 当有烯烃和酮存在时,有机金属试剂首先与烯烃反应
图 25. 醛和酮与有机金属试剂的反应
② 实施例2. Wittig反应:叶立德与醛和酮的加成反应
○ 叶立德试剂
○ 叶立德是指相邻原子极性相反的分子
○ 当P=C键形成时,P原子的内层d轨道电子参与成键,产生高能量,作为分离电荷的两性离子叶立德成为实际结构
图 26. 叶立德试剂
○ 叶立德试剂的制备:1. Ph3P, CH3Br, 2. BuLi
图 27. 叶立德试剂的制备
○ 实施例2-1. (通用) 酮中的O被C取代
图 28. Wittig 反应示例
○ 示例 2-2.

图 29. Wittig 反应示例
○ 优点:取代基较少的烯烃成为唯一产品
○ 缺点:Wittig反应生成的烯烃没有(E)/(Z)选择性,而图27.确实显示了选择性,值得注意
○ 解决方案
○ 如果叶立德亲核试剂的碳连接到吸电子基团(EWG)上,则反应活性较低,因此主要形成热力学稳定的烯烃。
○ 如果叶立德亲核试剂的碳连接到苯基上,则主要形成动力学有利(空间位阻较小)的烯烃。
③ 实施例3. Horner-Wadsworth-Emmons 反应
○ 选择性反应得到(E)-烯烃

图 30. Horner-Wadsworth-Emmons 反应的机理
④ 实施例4. Reformatsky反应
○ 与有机锌试剂的加成反应
○ 有机锌试剂反应性较低,不与酯基反应:与格氏试剂和酯不同
○ Reformatsky试剂形成后,醛和酮发生加成反应
<img src =“https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2FvMmnR%2Fbtrbqwh6rxV%2FL9LRcDlqII3fTGTgFqaoW0%2Fimg.png” alt=”绘图”>
图 31. Reformatsky 反应
⑤ 实施例5. 坎尼扎罗反应
○ 醛类无α-氢的强碱分子间氧化还原反应
○ 苯甲醛 + KOH + H2O → 苯甲酸钾(氧化)+ 苯甲醇(还原型)
图 32. Cannizzaro 反应机理
⑥ 实施例 6. Meerwein-Ponndorf-Verley 还原(Oppenauer 氧化)
○ Al(OC(CH3)3)3催化羰基还原和醇氧化
○ 相反反应称为奥本纳氧化
图 33. Meerwein-Ponndorf-Verley 还原(Oppenauer 氧化)
⑶ 沉淀反应:醛可以被进一步氧化,而酮则不能,导致沉淀反应的差异
① 银镜反应(托伦斯试验)
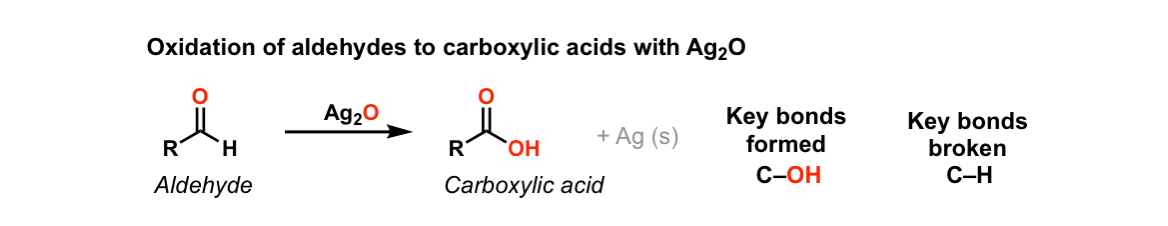
图 34. 银镜反应
○ Tollens 试剂:无色溶液
○ 步骤 1. 将 AgNO3 溶解在水中
○ 步骤 2. 添加 NaOH 或 KOH,使 Ag 沉淀为 Ag2O
○ 步骤3. 加入氨溶液,形成银氨络离子Ag(NH3)2+NO3-
○ 实验过程
○ 步骤1. 将还原物质加入硝酸银氨溶液(托伦斯试剂)中并加热
○ 步骤 2. 离子形式的银离子被还原,导致 Ag(s) 沉淀» ○ 还原糖:形成金属银
○ 醛:形成金属银
○ Ag2O 充当 Ag+ 供体:水中的氧移动到醛,从而产生羧酸。
○ 酮:无反应
○ 例外:与 α-羟基酮反应
○ 乙缩醛:无反应
○ 半缩醛:反应
○ 原因:半缩醛可裂解成羰基和醇基
② 费林反应
○ 斐林试剂:五水硫酸铜(CuSO4·5H2O)、NaOH、罗谢尔盐(酒石酸钠钾)
○ 实验过程
○ 步骤1. 将还原物质添加到费林溶液中并加热
○ 步骤 2. 用酒石酸还原离子形式的铜离子,导致氧化铜 (I) (Cu2O) 沉淀
○ 还原糖:形成铜沉淀(红棕色)
○ 脂肪醛:形成铜沉淀(红棕色)
○ 芳香醛:无反应
○ 酮:无反应
③ 本尼迪克特反应
○ 本尼迪克特溶液:CuSO4、Na2CO3、柠檬酸钠
○ 醛:形成铜沉淀(红棕色)
○ 酮:无反应
○ 不氧化肌酸和尿酸
○ 氧化葡萄糖、果糖、麦芽糖等:方便检测反应
⑷ 重排反应
① 实施例1. Baeyer-Villiger氧化:七元环结构的机理
○ 概述
○ 在过氧酸下,过量的氧转移至醛(或酮),生成羧酸(或酯)。
○ 重新排列期间保留配置。
○ 迁徙能力
○ H>苯基>叔烷基>环己基>仲烷基>伯烷基>甲基
○ 氧插入发生在富电子碳上(ref)
○ 1-1. 苯乙酮:苯环增强反应性
○ 苯乙酮与过氧化酸(RO3H)反应,例如CF3CO3H,形成乙酸苯酯
图 35. Baeyer-Villiger 氧化机制
考虑到-OH的氢,可以看出形成了七边形
○ 1-2. _m_CPBA
○ _m_CPBA 以 RCO3H 形式氧化酮
○ 氧插入发生在富电子碳上
○ 与烯烃的环氧化竞争,但Baeyer-Villiger反应占主导地位
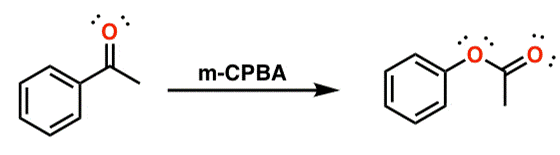
图 36. _m_CPBA 催化的 Baeyer-Villiger 氧化
② 示例 2. Tiffeneau-Demjanov 重排
○ 烷基重氮盐的形成导致不稳定并形成碳正离子
图 37. Tiffeneau-Demjanov 重排机制
③ 实施例3. Johnson-Corey-Chaykovsky 反应
○ 实施例 3-1. 使用硫叶立德的 Johnson-Corey-Chaykovsky 反应
○ 各类硫叶立德如下:
○ H2C-S(CH3)2: 硫叶立德(锍)
○ H2C-SO-(CH3)2: 科里叶立德(亚砜)
图 38. Johnson-Corey-Chaykovsky 反应机理
○ 实施例 3-2. 酮在 AlCl3、CH2N2 条件下的 Johnson-Corey-Chaykovsky 反应
图 39. 酮在 AlCl3、CH2N2 条件下的 Johnson-Corey-Chaykovsky 反应
○ 实施例3-3. 由于锍叶立德具有很强的亲核性,1,2-加成占主导地位
图 40. 1,2-锍叶立德的加成
○ 实施例 3-4. 由于亚砜叶立德是弱亲核试剂(∵酮基),因此 1,4-加成占主导地位
图 41. 1,4-亚砜叶立德的加成
> ④ 实施例4. 二苯甲酸重排
图42. 二苯乙醇酸重排机制
> ⑤ 实施例5. Favorskii重排反应
○(分子式) 强碱、酮、不饱和度增加一、除去两个离去基团
图 43. Favorskii 重排反应
4。醛合成方法
⑴ 烯烃的臭氧分解: 1. O3, 2. Zn, H2O 或 CH3SCH3
⑵ 末端炔烃的水合: 1. BH3, 2. H2O2, OH-
⑶ Gattermann-Koch反应合成苯甲醛:是一种甲酰基的Friedel-Crafts酰化反应。
⑷ 氯化苄与硝基甲烷阴离子的反应:氯化苄+硝基甲烷阴离子→苯甲醛
⑸ 伯醇的弱氧化:氧化为醛。
⑹ HIO4二醇的氧化裂解: HIO4, H2SO4
⑺【酰氯、酯类、腈类的还原】(https://jb243.github.io/pages/1380)
⑻ Reimer-Tiemann反应: CHCl3, KOH
⑼ Corey-Seebach反应: 硫缩醛 + HgCl2, MeOH, H2O → 醛
① 硫原子的作用:通过反键效应减少负电荷。硫原子容易极化,稳定负离子。
② Hg2+的作用:路易斯酸,六方铜结构溶剂
③ 没有Hg2+,逆反应占主导地位
5。酮合成方法
⑴【烯烃的臭氧分解】(https://jb243.github.io/pages/1363)
⑵【炔烃的水合】(https://jb243.github.io/pages/1363)
① 概述: 带有-OH基团的炔发生水合形成烯醇,然后烯醇发生互变异构生成酮。> ②酸催化水合反应: H2O, H2SO4 / H2O, H2SO4, HgSO4
③ 硼氢化-氧化反应: 1. BH3, 2. H2O2, OH- / 1. BH3, 2. H2O2, OH-
⑶ 傅克酰化
<img源= “https://img1.daumcdn.net/thumb/R1280x0/?scode=mtistory2&fname=https%3A%2F%2Fblog.kakaocdn.net%2Fdn%2FdrhOsf%2Fbtq8IDit7Ur%2FbiSJk5TKL3dUO6BWxQZdH0%2Fimg.png” alt=”绘图”>
图 44. 苯的傅克酰化
⑷【仲醇的氧化】(https://jb243.github.io/pages/1372)
⑸ HIO4二醇的氧化裂解: 1. HIO4, 2. H2SO4
⑹ Corey-Seebach反应: 硫缩酮 + HgCl2, MeOH, H2O → 醛
①硫原子的作用: 通过反键合效应减少负电荷。硫原子容易极化,稳定负离子。
② Hg2+的作用:路易斯酸,六方铜结构的溶剂化
③ 没有Hg2+,逆反应占主导地位
⑺【羧酸与有机锂试剂的反应】(https://jb243.github.io/pages/1380)
① 格氏试剂和吉尔曼试剂不与羧酸发生反应
⑻【酰氯与有机金属试剂的反应】(https://jb243.github.io/pages/1380)
⑼【腈类与有机金属试剂的反应】(https://jb243.github.io/pages/1380)
⑽ 【亚胺的酸催化水合反应】(https://jb243.github.io/pages/1386)
输入:2019.03.29 13:54
修改:2023.01.30 23:12































